กรดนิวคลีอิกของไวรัสไข้หวัดใหญ่/ไวรัสไข้หวัดใหญ่สายพันธุ์บีแบบแช่แข็งแห้ง
ชื่อผลิตภัณฑ์
ชุดตรวจหาดีเอ็นเอของไวรัสไข้หวัดใหญ่/ไวรัสไข้หวัดใหญ่สายพันธุ์บีแบบแช่แข็งแห้ง HWTS-RT193 (PCR แบบเรืองแสง)
ระบาดวิทยา
ตามความแตกต่างทางแอนติเจนระหว่างยีน NP และ M ไวรัสไข้หวัดใหญ่สามารถแบ่งออกได้เป็น 4 ประเภท ได้แก่ ไวรัสไข้หวัดใหญ่เอ (IFV A), ไวรัสไข้หวัดใหญ่บี (IFV B), ไวรัสไข้หวัดใหญ่ซี (IFV C) และไวรัสไข้หวัดใหญ่ดี (IFV D) สำหรับไวรัสไข้หวัดใหญ่เอ มีโฮสต์หลายชนิดและมีซีโรไทป์ที่ซับซ้อน และสามารถแพร่กระจายข้ามโฮสต์ได้ผ่านการรวมตัวทางพันธุกรรมและการกลายพันธุ์แบบปรับตัว มนุษย์ไม่มีภูมิคุ้มกันถาวรต่อไวรัสไข้หวัดใหญ่เอ ดังนั้นผู้คนทุกวัยจึงมีความเสี่ยงต่อการติดเชื้อ ไวรัสไข้หวัดใหญ่เอเป็นเชื้อก่อโรคที่สำคัญที่สุดที่ทำให้เกิดการระบาดใหญ่ของไข้หวัดใหญ่ สำหรับไวรัสไข้หวัดใหญ่บี ส่วนใหญ่แพร่กระจายในพื้นที่เล็กๆ และปัจจุบันยังไม่มีการแบ่งย่อยเป็นสายพันธุ์ย่อย การติดเชื้อในมนุษย์ส่วนใหญ่เกิดจากไวรัสไข้หวัดใหญ่สายพันธุ์ B/Yamagata หรือ B/Victoria จากจำนวนผู้ป่วยไข้หวัดใหญ่ที่ได้รับการยืนยันรายเดือนใน 15 ประเทศของภูมิภาคเอเชียแปซิฟิก อัตราการวินิจฉัยพบเชื้อไวรัสไข้หวัดใหญ่ชนิดบีมีตั้งแต่ 0 ถึง 92% ซึ่งแตกต่างจากไวรัสไข้หวัดใหญ่ชนิดเอ ตรงที่กลุ่มคนบางกลุ่ม เช่น เด็กและผู้สูงอายุ มีความเสี่ยงต่อการติดเชื้อไวรัสไข้หวัดใหญ่ชนิดบีได้ง่ายกว่า และสามารถก่อให้เกิดภาวะแทรกซ้อนได้ง่ายกว่า ส่งผลให้สังคมต้องรับภาระหนักกว่าการติดเชื้อไวรัสไข้หวัดใหญ่ชนิดเอเสียอีก
พารามิเตอร์ทางเทคนิค
| พื้นที่จัดเก็บ | 2-28℃ |
| อายุการเก็บรักษา | 12 เดือน |
| ประเภทตัวอย่าง | การเก็บตัวอย่างจากลำคอ |
| Ct | IFV A,IFVB Ct≤35 |
| CV | <5.0% |
| ระดับ LoD | 200 สำเนา/มล. |
| ความจำเพาะ | ปฏิกิริยาข้ามสายพันธุ์: ชุดตรวจนี้ไม่สามารถทำปฏิกิริยาข้ามสายพันธุ์กับไวรัส Bocavirus, Rhinovirus, Cytomegalovirus, Respiratory syncytial virus, Parainfluenza virus, Epstein-Barr virus, herpes simplex virus, varicella-zoster virus, Mumps virus, Enterovirus, Measles virus, human metapneumovirus, Adenovirus, human coronaviruses, novel coronavirus, SARS-CoV, MERS-CoV, Rotavirus, Norovirus, Chlamydia pneumoniae, Mycoplasma pneumoniae, Streptococcus pneumoniae, Klebsiella pneumoniae, Streptococcus pyogenes, Legionella, Pneumocystis jirovecii, Haemophilus influenzae, Bordetella pertussis, Staphylococcus aureus, Mycobacterium tuberculosis, Neisseria gonorrhoeae และ Candida ได้ อัลบิแคนส์, แคนดิดา กลาบราตา, แอสเพอร์จิลลัส ฟูมิแกตัส, คริปโตค็อกคัส นีโอฟอร์มานส์, สเตรปโตค็อกคัส ซาลิวาเรียส, โมแรกเซลลา คาตาร์ราลิส, แลคโตบาซิลลัส, คอรีเนแบคทีเรียม และดีเอ็นเอจีโนมของมนุษย์ การทดสอบการรบกวน: มิวซิน (60 มก./มล.), เลือดมนุษย์ (50%), ฟีนิลเอฟริน (2 มก./มล.), ออกซีเมทาโซลีน (2 มก./มล.), โซเดียมคลอไรด์ (20 มก./มล.) พร้อมสารกันเสีย 5%, เบคลอเมทาโซน (20 มก./มล.), เดกซาเมทาโซน (20 มก./มล.), ฟลูนิโซไลด์ (20 ไมโครกรัม/มล.), ไตรแอมซิโนโลน (2 มก./มล.), บูเดโซไนด์ (1 มก./มล.), โมเมทาโซน (2 มก./มล.), ฟลูติคาโซน (2 มก./มล.), ฮิสตามีนไฮโดรคลอไรด์ (5 มก./มล.), เบนโซเคน (10%), เมนทอล (10%), ซานามิเวียร์ (20 มก./มล.), เปรามิเวียร์ (1 มก./มล.), มูพิโรซิน (20 มก./มล.), โทบราไมซิน (0.6 มก./มล.), โอเซลทามิเวียร์ (60 นาโนกรัม/มล.), ริบาไวริน ได้เลือกสารละลายที่มีความเข้มข้น 10 มก./ลิตร มาทำการทดสอบการรบกวน และผลการทดสอบแสดงให้เห็นว่าสารรบกวนที่ความเข้มข้นดังกล่าวไม่มีปฏิกิริยารบกวนต่อผลการทดสอบของชุดทดสอบ |
| เครื่องมือที่เกี่ยวข้อง | ใช้ได้กับน้ำยาตรวจวิเคราะห์ประเภท I: ระบบ PCR แบบเรียลไทม์ Applied Biosystems 7500 ระบบ PCR แบบเรียลไทม์ SLAN-96P (บริษัท หงซือ เมดิคอล เทคโนโลยี จำกัด) ใช้ได้กับน้ำยาตรวจทดสอบประเภท II: ชุดทดสอบ EudemonTM AIO800 (HWTS-EQ007) ผลิตโดย Jiangsu Macro & Micro-Test Med-Tech Co., Ltd. |
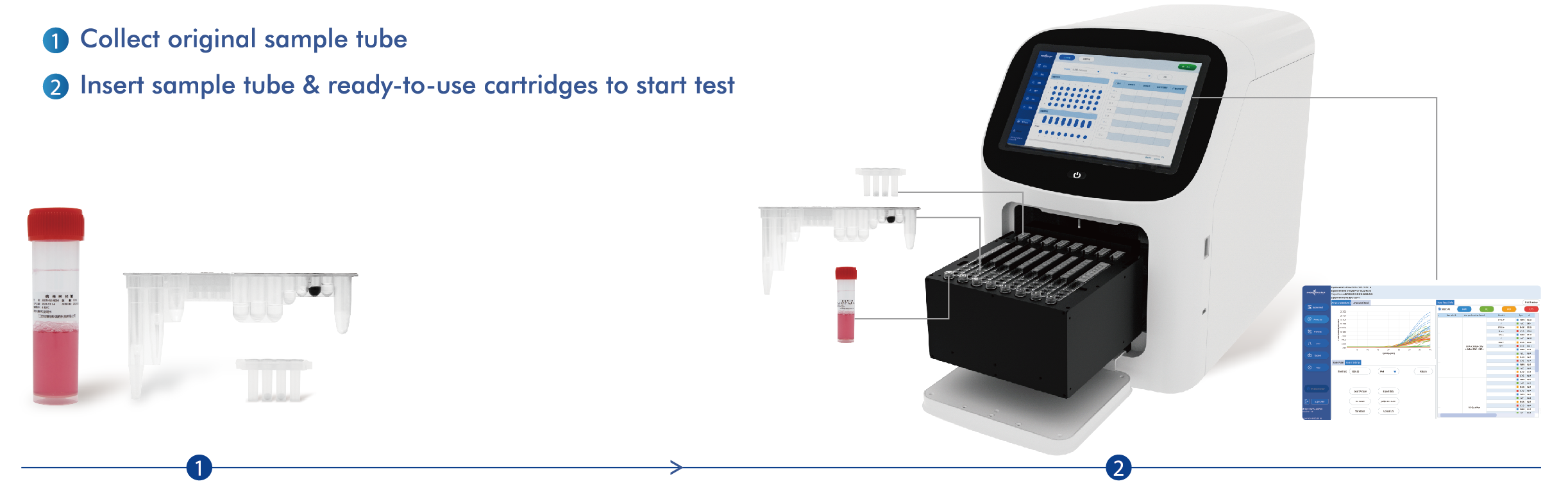
ขั้นตอนการทำงาน
พีซีอาร์แบบดั้งเดิม
ขอแนะนำให้ใช้ชุดตรวจ DNA/RNA ทั่วไปของ Macro & Micro-Test (HWTS-3019) (ซึ่งสามารถใช้ร่วมกับเครื่องสกัดกรดนิวคลีอิกอัตโนมัติของ Macro & Micro-Test (HWTS-3006C, (HWTS-3006B)) จากบริษัท Jiangsu Macro & Micro-Test Med-Tech Co., Ltd. ในการสกัดตัวอย่าง และขั้นตอนต่อไปควรดำเนินการอย่างเคร่งครัดตามคู่มือการใช้งานของชุดตรวจ
เครื่องออลอินวัน AIO800